פתרונות של אלקטרוליטים
פתרונות של אלקטרוליטים הם מיוחדיםנוזלים, אשר באופן חלקי או מלא בצורה של חלקיקים טעונים (יונים). עצם התהליך של פיצול מולקולות לשליליות (אניונים) וחלקיקים טעונים חיובי (קטיונים) נקרא דיסוציאציה אלקטרוליטית. דיסוציאציה בפתרונות מתאפשרת רק בשל יכולתם של יונים לקיים אינטראקציה עם מולקולות הנוזל הקוטבי, המפעילה כממס.
מה הם אלקטרוליטים?

פתרונות של אלקטרוליטים בהתאם לתוארניתוק יכול להיות מחולק חזק, בינוני וחלש. דרגת הדיסוציאציה (α) היא היחס בין מספר המולקולות שנרקבו לחלקיקים טעונים למספר הכולל של המולקולות. ב אלקטרוליטים חזקים, הערך של α גישות 1, עבור α 0.0 α בינוני, עבור α חלש <0.1.
אלקטרוליטים חזקים כוללים בדרך כלל מלחים, מספר חומצות מסוימות - HCl, HBR, HI, HNO3, ח2לכן4, HClO4, הידרוקסידים של בריום, סטרונציום, סידן ומתכות אלקליות. בסיסים אחרים וחומצות הם אלקטרוליטים בינוניים או חלשים.
תכונות של פתרונות אלקטרוליטים
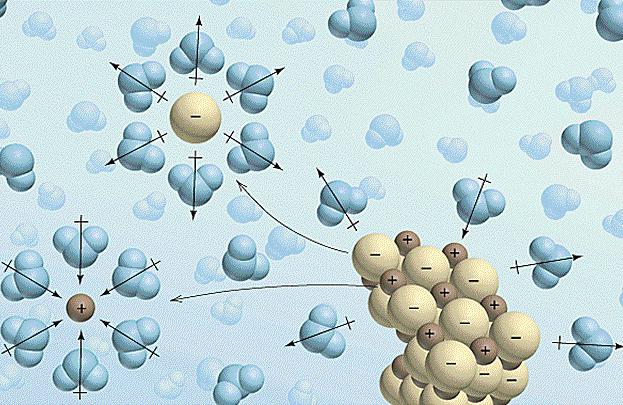
- הרס הקשרים הבין-מולקולריים והכימיים של אלקטרוליט מומס מחייב את ההוצאות של כמות מסוימת של אנרגיה, ולכן, ספיגת החום מתרחשת (ΔHexp > 0).
- בשלב זה, הממס מתחילאינטראקציה עם יונים של אלקטרוליט, וכתוצאה מכך היווצרות של solvates (ב מימית פתרונות - hydrates). תהליך זה נקרא הפיתרון והוא אקסותרמי, א. יש שחרור חום (ΔHהידרא <0).
- השלב האחרון הוא דיפוזיה. זוהי התפלגות אחידה של hydrates (solvates) בפתרון בתפזורת. תהליך זה דורש עלויות אנרגיה ולכן הפתרון הוא מקורר (ΔHהבדל > 0).
לכן, ההשפעה התרמית הכוללת של המסת אלקטרוליט ניתן לכתוב בצורה זו:
Δayraststv 49 Δayexp + ΔНהידרא + ΔНהבדל
הסימן הסופי של אפקט תרמי הכולל של המסת אלקטרוליט תלוי מה ההשפעות האנרגיה המרכיבים להתברר להיות. בדרך כלל תהליך זה הוא אנדותרמי.

בהתאם מומסחומרים, כל הפתרונות של אלקטרוליטים ניתן לחלק לדלל מאוד (המכיל רק "עקבות" של אלקטרוליט) מדולל (עם תוכן קטן של מומס) מרוכז (עם תוכן משמעותי של אלקטרוליט).
תגובות כימיות בפתרונות אלקטרוליטים,אשר נגרמות על ידי מעבר של זרם חשמלי, להוביל לשחרור של חומרים מסוימים על האלקטרודות. תופעה זו נקראת אלקטרוליזה והיא משמשת לעתים קרובות בתעשייה המודרנית. בפרט, הודות אלקטרוליזה, אלומיניום, מימן, כלור, hydroxide נתרן, מי חמצן וחומרים חשובים אחרים מתקבלים.


